حل الفصل الثالث سرعة التفاعلات الكيميائية كتاب كيمياء 3 للمرحلة الثانوية و حلول كتاب الكيمياء 3 المرحلة الثانوية للعام الدراسي 1442 هـ.
يتضمن الفصل الثالث ثلاثة دروس هي على الترتيب: نظربة التصادم وسرعة التفاعل الكيميائي - العوامل المؤثرة في سرعة التفاعل الكيميائي - قوانين سرعة التفاعل الكيميائي، بالإضافة إلى تقويم الفصل.
الفصل الثالث سرعة التفاعلات الكيميائية
نكمل معكم باستعراض حلول الفصل الثالث في حل كتاب كيمياء 3 مقررات ثانوي وهو ثالث فصول الكتاب لهذا الفصل الدراسي.
حل درس نظربة التصادم وسرعة التفاعل الكيميائي
مسائل تدريبية
استعمل البيانات الموجودة في الجدول أدناه لحساب متوسط سرعة التفاعل :
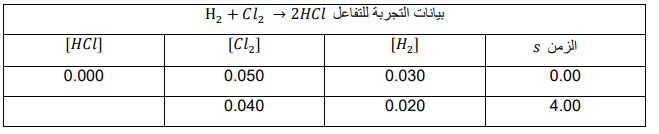
السؤال : احسب متوسط سرعة التفاعل معبراً بعدد مولات 2 𝐻 المستهلكة لكل لتر في كل ثانية
الجواب :
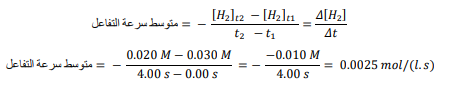
السؤال : احسب متوسط سرعة التفاعل معبراً بعدد مولات 2 𝐶𝑙المستهلكة لكل لتر في كل ثانية. ؟
الجواب :
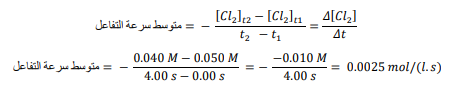
السؤال : تحفيز إذا علمت أن متوسط سرعة التفاعل لحمض الهيدروليك HCLالناتج هو 0.050mol/l، فما تركيز HClالذي يتكون بعد مرور 4.00s
الجواب : تكون HCl لذا سيكون تعبير متوسط سرعة التفاعل موجبا
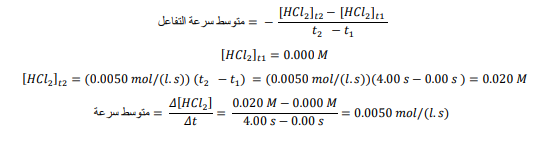
التقويم
السؤال : جد العلاقة بين نظرية التصادم وسرعة التفاعل ؟
الجواب :تفسر نظرية التصادم كيفية حدوث التفاعلات ، وكيفية تعديل سرعة التفاعل وحتى يحدث التفاعل يجب أن تتصادم الجزيئات ، أو الذرات ، أو الأيونات ، حيث يحدد تر دد ودوران وطاقة هذه التصادمات متوسط سرعة التفاعل الكلي
السؤال : فسر علام تدل سرعة التفاعل لتفاعل كيميائي محدد ؟
الجواب : تبين سرعة التفاعل التغير في تراكيز المواد المتفاعلة أو الناتجة بوحدة mol/(l.s)
السؤال : قارن بين تراكيز المواد المتفاعلة والمواد الناتجة خلال فترة التفاعل ( على افتراض عدم إضافة أي مادة جديدة )
الجواب : تتناقص تراكيز المواد المتفاعلة ، في حين تتزايد تراكيز المواد الناتجة بالسرعة نفسها
السؤال : فسر لماذا يعتمد متوسط سرعة التفاعل على طول الفترة الزمنية اللازمة لحدوث التفاعل ؟
الجواب : علاقة التغير في سرعة المواد المتفاعلة والناتجة ليست علاقة خطية مع الزمن يتناقص متوسط سرعة التفاعل عندما يتناقص تركيز المواد المتفاعلة حيث يتناسب متوسط التغير في سرعة التفاعل تناسبا طرديا مع تراكيز المواد المتفاعلة لذا كلما ازدادت الفترة الزمنية للتفاعل قلت قيمة متوسط التغير في سرعته
السؤال : صف العلاقة بين طاقة التنشيط وسرعة التفاعل الكيميائية ؟
الجواب : يقل متوسط سرعة التفاعل كلما ازدادت طاقة التنشيط
السؤال : لخص اذا يحدث خلال فترة تكون المعقد النشط القصيرة ؟
الجواب : تنكسر الروابط في المواد المتفاعلة ، في حين تتشكل روابط جديدة لتكون النواتج
السؤال :طبق نظرية التصادم لتفسير لماذا لا تؤدي الاصطدامات بين جسيمات التفاعل دائم إلى تفاعل ؟
الجواب : يجب أن يحدث التصادم في اتجاه مناسب ، وامتلاك الطاقة الكافية لتكوين المعقد المنشط
السؤال : احسب متوسط سرعة التفاعل بين جزيئات A و B إذا تغير تركيز A من M 00.1 إلى 0.5M خلال 2.00s
الجواب :

حل درس العوامل المؤثرة في سرعة التفاعل الكيميائي
التقويم 3-2
السؤال : فسر سبب تفاعل فلز الماغنسيوم مع حمض الهيدروليك HCl أسرع من الحديد
الجواب : يعد فلز الماغنسيوم أكثر نشاطاً من الحديد ، لذا سيكون تفاعل الماغنسيوم مع HCl أسرع من تفاعل الحديد معه .
السؤال : فسر كيف تفسر نظرية التصادم تأثير التركيز في سرعة التفاعل ؟
الجواب : - يؤدي ازدياد تركيز المواد المتفاعلة إلى زيادة عدد التصادمات بين جسيمات المواد المتفاعلة مما يؤدي إلى زيادة سرعة التفاعل
السؤال : فسر الفرق بين المحفزات والمثبطات .؟
الجواب : المحفزات تزيد من سرعة التفاعل وذلك بخفض طاقة التنشيط ، في حين تبطئ المثبطات التفاعل ، أو توقفه أحياناً وذلك بالتدخل في المواد المتفاعلة أو المحفزات .
السؤال : صف تأثير طحن إحدى المواد الداخلة في التفاعل على شكل مسحوق بدلا من وضعها قطعة واحدة- في سرعة التفاعل .
الجواب : عند طحن إحدى المواد الداخلة في التفاعل على شكل مسحوق فإن ذلك يزيد من مساحة سطح التفاعل مما يزيد من عدد الصطدامات بين الجسيمات المتفاعلة فتزداد سرعة التفاعل .
السؤال : استنتج إذا كانت زيادة درجة حرارة التفاعل بمقدار 10 K يؤدي إلى تضاعف سرعة التفاعل ، فماذا تتوقع أن يكون أثر زيادة درجة الحرارة بمقدار K20 ؟
الجواب : ستزداد سرعة التفاعل بمقدار 4 أضعاف عن سرعة التفاعل الأصلية .
السؤال : ابحث في كيفية استعمال المحفزات في الصناعة ، أو الزراعة ، أو في معالجة التربة الملوثة ، أو النفايات ، أو الماء الملوث . اكتب تقريراً قصيراً يلخص النتائج التي حصلت عليها حول دور المحفزات في إحدى هذه التطبيقات .
الجواب : يجب أن يظهر في التقرير أن : المحفز يزيد من سرعة التفاعل ، ولا يستهلك فيه .
الفصل الثالث الدرس 3-3
مسائل تدريبية
السؤال : اكتب معادلة قانون سرعة التفاعل bB → aA إذا كان تفاعل المادة A من الرتبة الثالثة .
الجواب :
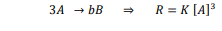
السؤال : إذا علمت ان التفاعل
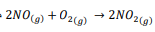
من الرتبة الأولى بالنسبة للأكسجين والرتبة الكلية للتفاعل هي الرتبة الثالثة ، فما القانون العام لسرعة التفاعل ؟
الجواب :
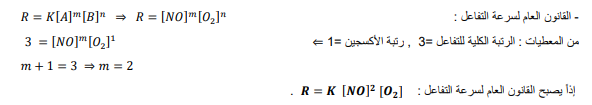
السؤال : في ضوء البيانات التجريبية الواردة في الجدول الآتي ، حدد قانون سرعة التفاعل : نواتج bB + aA
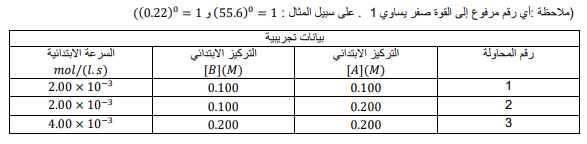
الجواب : بدراسة المحاولتين 2 و 1 سنجد أن مضاعفة تركيز [A] ال يؤثر في سرعة التفاعل ، لذا فإن رتبة التفاعل للمادة A تساوي صفرا .بدراسة المحاولتين 2 و 3 فإن مضاعفة تركيز المادة [B] يؤدي إلى مضاعفة سرعة التفاعل ، لذا فرتبة التفاعل أحادية بالنسبة للمادة B
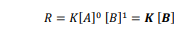
السؤال : تحفيز إذا عملت أن قانون سرعة التفاعل
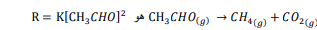
فاستعمل هذه المعلومات لتعبئة البيانات المفقودة في الجدول الآتي :
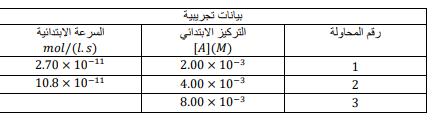
الجواب : بدراسة المحاولتين 2 و 1 : تؤدي مضاعفة تركيز CH3CHOإلى زيادة سرعة التفاعل بمقدار المعامل 4، وبدراسة المحاولتين 2 و 3 : نجد أن مضاعفة تركيز المادة [B] سيؤدي إلى مضاعفة سرعة التفاعل أيضاً بمقدار المعامل 4.: لذا فالسرعة في المحاولة 3 هي :
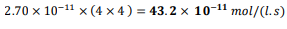
التقويم 3-3
السؤال : اشرح ماذا يمكن أن نعرف عن التفاعل من خلا ل قانون سرعة التفاعل الكيميائي ؟
الجواب : من قانون سرعة التفاعل الكيميائي يمكن معرفة رتبة التفاعل حيث أن :
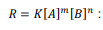
حيث [A] ,[ B ] تركيز المواد المتفاعلة، m رتبة التفاعل A ،n رتبة التفاعل B .والرتبة الكلية للتفاعل = m+n
السؤال : طبق اكتب معادلات قانون سرعة التفاعل التي تظهر الفرق بين التفاعل من الرتبة الأولى والتفاعلمن الرتبة الثانية لمادة متفاعلة واحدة .
الجواب :
إذا كان التفاعل من الرتبة األولى تكون المعادلة : R=K[A]
إذا كان التفاعل من الرتبة الثانية فتكون المعادلة : R=K[A]2
السؤال : اشرح وظيفة ثابت سرعة التفاعل في معادلة قانون سرعة التفاعل
الجواب : ثابت سرعة التفاعل هو قيمة عددية تربط سرعة التفاعل بتركيز المواد المتفاعلة عند درجة حرارة معينة.
السؤال : اشرح متى يمكن أن يصبح ثابت سرعة التفاعل K ليس ثابتاً ؟ وعالم تدل قيمة K في قانون سرعة التفاعل ؟
الجواب : يصبح ثابت السرعة K ليس ثابتاً عند تغير درجة الحرارة وتدل قيمة K على سرعة تفاعل المواد المتفاعلة لتكوين المواد الناتجة.
السؤال : اقترح تفسيراً لأهمية أن نعرف أن قيمة قانون سرعة التفاعل هو متوسط سرعة التفاعل
الجواب : بذلك نستطيع أن نعبر عن سرعة التفاعل بخطوة واحدة .
السؤال : اشرح كيفية ارتباط لأسس في معادلة قانون سرعة تفاعل كيميائي بالمعاملات في المعادلة الكيميائية التي تمثله .
الجواب : الأسس في قانون سرعة التفاعل الكيميائي هي المعاملات في المعادلة الكيميائية ،
فإذا كانت المعادلة الكيميائية هي : نواتج → bB+aA . فإن معادلة قانون السرعة التي تمثل هذا التفاعل هي : R=K[A] m[B]n حيث n=b-m=a
السؤال : حدد الرتبة الكلية لتفاعل المادتين A و B إذا علمت أن معادلة سرعته : R=K[A]2[B]2
الجواب : الرتبة الكلية للتفاعل = مجموع رتب المواد المتفاعلة = 2 + 2 = 4
السؤال : صمم تجربة اشرح كيف يمكن تصميم تجربة لتحديد القانون العام لسرعة التفاعل باستعمال طريقة مقارنة السرعات االبتدائية للتفاعل :نواتج → bB+aA
الجواب :
بإجراء تفاعل بين المواد A , Bوقياس السرعة الابتدائية ، وثم لتحديد رتبة المادة A ، تقاس سرعة التفاعل لعدة محاولات ، حيث تتغير قيمة [A] في كل مرة في حين تبقى قيمة [B] ثابتة ، ولتحديد رتبة المادة المتفاعلةB : تقاس سرعة التفاعل عدة مرات باعتبار تغّير قيمة [B] في حين تبقى قيمة [A] ثابتة .
الفصل الثالث الدرس ( التقويم )
إتقان المفاهيم
السؤال : ماذا يحدث لتراكيز المواد المتفاعلة والناتجة أثناء حدوث التفاعل ؟
الجواب : يقل تراكيز المواد المتفاعلة ، في حين يزداد تركيز المواد الناتجة .
السؤال : اشرح المقصود بمتوسط سرعة التفاعل .؟
الجواب : متوسط سرعة التفاعل هو التغير في تركيز المواد المتفاعلة أو الناتجة خلال فترة زمنيّة محددة .
السؤال : كيف يمكن أن تعبر عن سرعة التفاعل الكيميائي B → A بالاعتماد على تركيز المادة A ؟ وكيف يمكن مقارنة سرعة التفاعل باالعتماد على المادة الناتجة B ؟
الجواب :

السؤال : ما دور المعقد النشط في التفاعل الكيميائي ؟
الجواب : يعد المعقد النشط حالة وسطية بين المواد المتفاعلة والمواد الناتجة ، حيث أنه قد يؤدي إلى تكوين المواد الناتجة أو ينكسر ليكون المواد المتفاعل مرة أخرى .
السؤال : فترض أن جزيئين قد يتفاعلان إذا تصادما ، فتحت أي ظرف يمكن أن لا يتفاعلا ؟
الجواب : عند عدم توافر الطاقة الكافية اللازمة لحدوث التفاعل ، لذا لاتؤدي التصادمات بين الجزيئات في هذه الحالة إلى تفاعل , إذا لم يتوافر الاتجاه المناسب لحظة التصادم
إتقان المسائل
السؤال : يتفاعل الماغنسيوم مع حمض الهيدروليك حسب المعادلة :
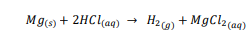
إذا كانت كتلة Mg تساوي g 0.60 لحظة بدء التفاعل ، وبقي منها 4.5g بعد مضي min 00.3 فما متوسط سرعة التفاعل بدلالة عدد Mg مولات المستهلكة/ دقيقة ؟
الجواب :

السؤال : ان وجد سرعة تفاعل كيميائي 2.25×10mol/l عند درجة حرارة 322k فما مقدار هذه السرعة بوحدة mol/l.min
الجواب : نضرب في معامل التحويل min=60s
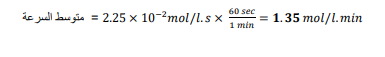
إتقان المفاهيم
السؤال : ما دور نشاط المواد المتفاعلة في تحديد سرعة التفاعل الكيميائي ؟
الجواب : تعتمد سرعة الفاعل على نشاط المواد المتفاعلة ، وتكون المواد المتفاعلة ذات النشاط الأعلى تحت ظروف معينة هي الأسرع تفاعلا.
السؤال : ما العلاقة بين سرعة التفاعل عموماً وتركيز المواد المتفاعلة ؟
الجواب : كلما ازداد تركيز المواد المتفاعلة يزداد عدد الاصطدامات مما يؤدي إلى زيادة سرعة التفاعل الكيميائي. في حين يؤدي تقليل التركيز إلى تقليل السرعة .
السؤال : طبق نظرية التصادم لتفسير سبب زيادة سرعة التفاعل بزيادة تركيز المادة المتفاعلة
الجواب : عندما يزداد تركيز المواد المتفاعلة تزداد عدد جزيئات المواد المتفاعلة مما يزيد من عدد الاصطدامات فتزداد سرعة التفاعل الكيميائي
السؤال : فسر لماذا تتفاعل المادة الصلبة – التي على شكل مسحوق- مع الغاز أسرع من تفاعل المادة الصلبة نفسها إذا كانت قطعة واحدة ؟
الجواب : لان المادة على شكل مسحوق يزداد فيها مساحة السطح المعرضة للتفاعل عن تلك التي على شكل قطعة واحدة مما يزيد من عدد الاصطدامات بين الجسيمات المتفاعلة فتزداد سرعة التفاعل .
السؤال : حفظ الأغذية طبق نظرية التصادم لتفسير فساد الطعام ببطء عند وضعه في الثلاجة بالمقارنة مع بقائه خارجها عند درجة حرارة الغرفة
الجواب : لان سرعة التفاعل تزداد بزيادة درجة الحرارة وتقل عندما تقل درجة الحرارة فعند وضع الطعام في الثالجة تقل درجة الحرارة ( يقل عدد التصادمات بين المواد المتفاعلة ) فتقل سرعة التفاعلات التي تسبب فساد الطعام بالمقارنة بسرعة هذه التفاعلات عند درجة حرارة الغرفة.
السؤال : طبق نظرية التصادم لتفسير سبب تفاعل مسحوق الخارصين لإنتاج غاز الهيدروجين أسرع من تفاعل قطع كبيرة منه عند وضع كليهما في محلول حمض الهيدروليك .
الجواب : عندما يكون الخارصين على شكل مسحوق فذلك يزيد من مساحة سطح الخارصين المعرضة للتفاعل أكثر منها في حالة القطعة الواحد مما يزيد من عدد االصطدامات بين الجسيمات فيزيد من سرعة التفاعل.
السؤال : يتحلل فوق أكسيد الهيدروجين إلى ماء وغاز لأكسجين بسرعة أكبر عند إضافة ثاني أكسيد المنجنيز . اشرح دور ثاني أكسيد المنجنيز في هذا التفاعل إذا علمت أنه لا يستهلك في التفاعل .
الجواب : يعد ثاني اكسيد المنجنيز محفز لتفاعل التحلل لأنه يؤدي تقليل طاقة التنشيط
إتقان المسائل
السؤال : نفترض أن كمية كبيرة من محلول فوق أكسيد الهيدروجين الذي تركيزه %3 قد تحلل لإنتاج 12ml من غاز الأكسجين خالل 100 ثانية عند درجة حرارة 298 K قدر كمية غاز الأكسجين التي تنتج عن مقدار مماثل من المحلول في 100 ثانية وعند درجة حرارة k 308.
الجواب : تتضاعف سرعة التفاعل لكل زيادة في درجة الحرارة مقدارها K10 . لذا سينتج 24 ml = (2 × 12 )من غاز الاكسجين .
السؤال : استعمل المعلومات في السؤال 44 لتقدير كمية غاز الأكسجين التي تنتج عن كمية مماثلة من المحلول خلال 100 ثانية وعند درجة حرارة K 318 ، ثم قدر الزمن اللازم لإنتاج 12 ML من غاز الاكسجين عند درجة حرارة 288k
الجواب : - تتضاعف سرعة التفاعل لكل زيادة في درجة الحرارة مقدارها K 10 . لذا سينتج 12×2=2ml من غاز الاكسجين
السؤال : استعمل المعلومات في السؤال 33 لتقدير كمية غاز الاكسجين التي تنتج عن كمية مماثلة من المحلول خلال 100 ثانية وعند درجة حرارة 318 K ثم قدر الزمن اللازم لإنتاج 12 ML من غاز الاكسجين عند درجة حرارة 288 K
الجواب :
تتضاعف سرعة التفاعل لكل زيادة في درجة الحرارة مقدارها K 10 . لذا سينتج ML48 = ( 2 × 24 من غاز الأكسجين . - وتقل سرعة التفاعل بمقدار النصف لكل انخفاض مقداره K 10، لذلك لكي نحصل على كمية الأكسجين نفسها نضاعف الزمن إلى ) s 200)
إتقان المفاهيم
السؤال : عند اشتقاق قانون سرعة التفاعل ، فسر لماذا يجب الاعتماد على الأدلة التجريبية أكثر من الاعتماد على المعادلات الكيميائية الموزونة للتفاعل ؟
الجواب : لأن معظم التفاعلات الكيميائية تحدث بأكثر من خطوة ، و لأن ثابت السرعة له قيمة محددة لكل تفاعل يتم تحديدها تجريبيا
السؤال : إذا كانت معادلة التفاعل العام هي AB → B + A وقد وجد بالاعتماد على البيانات التجريبية أن رتبة التفاعل من الرتبة الثانية بالنسبة للمادة المتفاعلة A ، فكيف تتغير سرعة التفاعل إذا انخفض تركيز المادة A إلى النصف ، وبقيت جميع الظروف الأخرى ثابتة ؟
الجواب : رتبة التفاعل بالنسبة للمادة n=2:A. إذا انخفض تركيز المادة A إلى النصف إذا سرعة التفاعل = ½ =¼ أي ان سرعة التفاعل سوف تقل إلى ربع قيمتها الابتدائية
إتقان المسائل
السؤال : تم الحصول على البيانات التجريبية في الجدول 4 ـ3 من تحلل مركب الازوميثان CH3N2CH3 عند درجة حرارة محددة حسب المعادلة
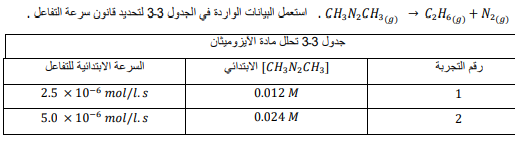
الجواب : من الجدول 3-3 عند زيادة تركيز الازوميثان إلى الضعف تزداد سرعة التفاعل إلى الضعف أيضا لذا التفاعل من التربة الاولى R=K[CH3N2CH3]
السؤال : استعمل بيانات الجدول 3-3 لحساب قيمة ثابت سرعة التفاعل K
الجواب :
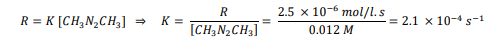
السؤال : استعمل بيانات الجدول 3 ـ 3 لتوقع سرعة التفاعل ، إذا كان التركيز الابتدائي ل 3𝐶𝐻2𝑁3 𝐶𝐻هوM 048.0 ، ودرجة الحرارة ثابتة.
الجواب : تزداد تركيز عن المحاولة 3 بمقدار الضعف ولذلك يزداد سرعة التفاعل الابتدائية إلى مقدار الضعف لان التفاعل من الرتبة الاولى ,
𝑅 = 𝐾 [𝐶𝐻3𝑁2𝐶𝐻3 ] = 2.5 × 10−6 × 2 = 1.0 × 10−5 𝑚𝑜𝑙/𝑙.
مراجعة عامة
السؤال : قوم صحة الجملة الآتية : يمكنك تحديد سرعة تفاعل كيميائي عن طريق معرفة نسبة مولات المواد المتفاعلة في معادلة موزونة . فسر إجابتك .
الجواب : الجملة غير موثوقة ، لأن معظم التفاعلات الكيميائية تحدث في صورة سلسلة من الخطوات الابتدائية ، ويجب أن يحدد قانون سرعة التفاعل وفق الطريقة التجريبية
السؤال : يتناقص تركيز المادة المتفاعلة A من 0.400mol/l إلى 0.384mol/l خلال 4.00min
احسب متوسط سرعة التفاعل خلال هذه الفترة بوحدة mol/l.min
الجواب :

السؤال : إذا زاد تركيز إحدى المواد الناتجة من 0.0882mol/l إلى0.1446خلال 12.0min فما متوسط سرعة التفاعل خلال تلك الفترة ؟
الجواب :

السؤال : يعبر عن التركيز في التفاعل الكيميائي بوحدة mol/l وعن الزمن بوحدة s . فإذا كان التفاعل الكلي من الرتبة الثالثة ، فما وحدة ثابت سرعة التفاعل ؟
الجواب :
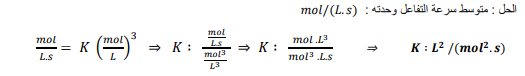
التفكير الناقد
السؤال : ميز بين المناطق المظللة في الشكل 15 ـ 3 عند درجتي الحرارة 1 𝑇و 2 𝑇بالاعتماد على عدد الاصطدامات التي تحدث في وحدة الزمن والتي لها طاقة أكبر من أو تساوي طاقة التنشيط
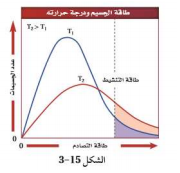
. الجواب : المنطقة المظللة تحت المنحنى تمثل عدد االصطدامات التي لها طاقة متساوية أو أكبر من طاقة التنشيط. فعند 2 𝑇درجة الحرارة العالية عدد االصطدامات العالية الطاقة أكبر بكثير من عدد الاصطدامات عند درجة الحرارة المنخفضة T1.
السؤال : تأمل مخطط الطاقة لتفاعل ماص للطاقة ، مكون من خطوة واحدة ، ثم قارن ارتفاع طاقة التنشيط للتفاعل الامامي والتفاعل العكسي .
الجواب : طاقة التنشيط للتفاعل الأمامي أكبر من طاقة التنشيط للتفاعل العكسي
السؤال : طبق طريقة مقارنة السرعات الابتدائية لتحديد رتبة التفاعل الكيميائي بالنسبة للمادة المتفاعلة X. واكتب مجموعة البيانات التجريبية الافتراضية التي تقود إلى استنتاج أن تفاعل المادة X من الرتبة الثانية .
الجواب :
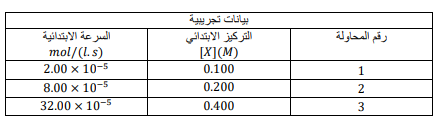
بدراسة المحاولتين 1 و 2 فإن مضاعفة تركيز المادة [X ] يؤدي إلى مضاعفة سرعة التفاعل 4 أضعاف ، 4 = 2 فإن قيمة n = 2 , لذا فرتبة التفاعل ثنائية بالنسبة للمادة X . وبدراسة المحاولتين 1 و 3 فإن مضاعفة تركيز المادة [X] 4 أضعاف يؤدي إلى مضاعفة سرعة التفاعل 16 ضعف ، 16 = 4 =n , فإن قيمة n = 2 , لذا أيضا يتأكد معنا أن رتبة التفاعل ثنائية بالنسبة للمادة x
R=K[X]2
السؤال : طبق نظرية التصادم لتفسير سببين لماذا تؤدي الزيادة في درجة حرارة التفاعل بمقدار K 10 غالباً إلى مضاعفة سرعة التفاعل
الجواب :
1- إن زيادة درجة الحرارة بقدار K 10 ، تزيد من متوسط سرعة تفاعل الجسيمات وعليه تزاد وتيرة التصادمات .
2- تزداد أيضاً عدد التصادمات التي لها طاقة كافية لتكوين المعقد المنشط بمقدار الضعف في معظم الأحيان .
السؤال : ارسم مخططاً يبين جميع االحتماالت للتصادمات بين جزيئين من المادة المتفاعلةA، وجزيئين من المادة المتفاعلة B. ثم زد عدد جزيئات A من 2إلى 4 ، وارسم جميع احتمالات التصادم التي يتحد فيها A مع B . كم سيزداد عدد التصادمات التي ينتج عنها اتحاد A مع B ؟ وعالم يدل ذلك فيما يتعلق بسرعة التفاعل ؟
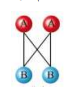
الجواب :
في البداية كان عدد التصادمات بين A و B ( 4 ) عند زيادة عدد الجزيئات : سيزداد عدد التصادمات بين من 4 إلى 8 أي ما يساوي الضعف ، وبما أن سرعة التفاعلات تعتمد على عدد التصادمات ، فستتضاعف السرعة على الأرجح .
السؤال : صمم جدولا لكتابة تراكيز المواد المتفاعلة في المعادلة التالية مبتدئا ب 0.100M لكل المتفاعلات . ثم حدد قانون سرعة التفاعل باستعمال طريقة مقارنة السرعات الابتدائية
نواتج → aA + bB +cD
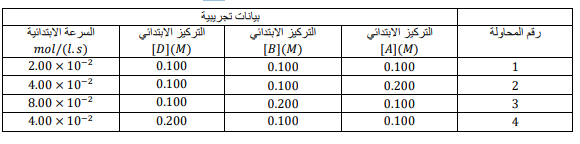
الجواب :
بدراسة المحاولتين 1 و 2 فإن مضاعفة تركيز المادة [A] يؤدي إلى مضاعفة سرعة التفاعل ، لذا فرتبة التفاعل أحادية بالنسبة للمادة A وبدراسة المحاولتين 1 و 3 فإن مضاعفة تركيز المادة [B] يؤدي إلى مضاعفة سرعة التفاعل 4 أضعاف ،لان 4 = 2 فإن قيمة n =2 , لذا فرتبة التفاعل ثنائية بالنسبة للمادة لا . بدراسة المحاولتين 1 و 4 فإن مضاعفة تركيز المادة [D] يؤدي إلى مضاعفة سرعة التفاعل ، لذا فرتبة التفاعل أحادية بالنسبة للمادة D . وبالتالي فإن قانون سرعة التفاعل
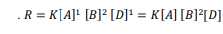
مسألة تحد
السؤال : الهيدروكربونات . يتحول البروبان الحلقي C3H6عند تسخينه إلى بروبين CH2=CHCH3 فإذا علمت أن سرعة التفاعل من الرتبة الاولى بالنسبة للبروبان الحلقي ، وكان ثابت السرعة عند درجة حرارة معينة 10 × 22.6 وثبت تركيز البروبان الحلقي عند 0.300mol/l ، فما كتلة البروبين الناتجة خلال 10.0minفي حجم مقداره L2.50 ؟
الجواب : نحسب متوسط سرعة التفاعل ، ثم تحسب كتلة البروبين الناتجة :
مراجعة تراكمية
السؤال : ما كتلة كلوريد الحديد III اللازمة لتحضير محلول مائي منه حجمه 1.0L وتركيزه M 225.0 ؟

الجواب : نحسب الكتلة المولية لكلوريد الحديد III . FeCL3

السؤال : ما المعلومات التي ينبغي معرفتها لحساب االرتفاع في درجة غليان محلول الهكسان في البنزين ؟
الجواب : مولارية المحلول ، وثابت الارتفاع في درجة غليان البنزين .
السؤال : إذا كانت H𝛥 لتفاعل ما سالبة . فقارن طاقة المواد الناتجة بطاقة المواد المتفاعلة ، وهل التفاعل ماص أم طارد للطاقة ؟
الجواب : طاقة المواد المتفاعلة أعلى من طاقة المواد الناتجة ، والتفاعل عندها طارد للطاقة .
تقويم إضافي
الكتابة في الكيمياء
السؤال : الأدوية تخيل انتشار مرض الانفلونزا في بلد ما ؟
الجواب : ولحسن الحظ قام العلماء باكتشاف محفز جديد يزيد من سرعة إنتاج دواء فعال ضد هذا المرض . اكتب مقالا صحفياً يصف كيفية عمل هذا المحفز على أن يشمل المقال مخطط الطاقة في التفاعلات التي تحدث ، وشرحاً مفصلا لأهمية هذا الاكتشاف - يجب ان يتضمن المقال وصفا لطريقة عمل المحفزات و مخطط طاقة للتفاعل ، ووصف مفصل لأهمية هذا الاكتشاف
أسئلة المستندات
الكواشف الكيميائية يستعمل الكاشف الكيميائي( الفينولفثالين ) للكشف عن القواعد .
تبين بيانات الجدول 3ـ3 انخفاض تركيز الفينولفثالين مع مرور الزمن عند إضافة محلول الفينولفثالين ذا التركيز M 050.0 إلى محلول مركز من مادة قاعدية تركيزها M 6.0
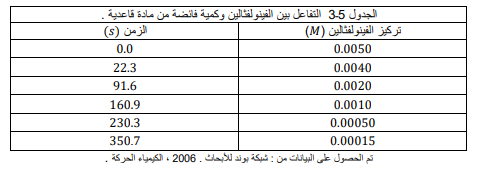
السؤال : ما متوسط سرعة التفاعل في أولs 3.22 معبراً عنه بوحدة (L.S)/ MOL ؟
الجواب :

السؤال : ما متوسط سرعة تفاعل الفينولفثالين عندما ينخفض تركيزه من M 00050.0 إلى 00015.0 ؟
الجواب :

اختبار مقنن
أسئلة الاختيار من متعدد
السؤال : جميع العبارات التالية حول سرعة التفاعل الكيميائي صحيحة ما عدا :
a .السرعة التي يحدث بها التفاعل .
b .التغير في تراكيز المواد المتفاعلة خلال وحدة الزمن .
c .التغير في تراكيز المواد الناتجة خلال وحدة الزمن
d .كمية المواد الناتجة المتكونة في كل فترة زمنية .
الجواب :d .كمية المواد الناتجة المتكونة في كل فترة زمنية .
السؤال : ادرس العبارات التالية :
العبارة الاولى : من العوامل التي تؤثر في سرعة التفاعل : طبيعة المادة المتفاعلة ، والتركيز ، ومساحة السطح التفاعل ، ودرجة الحرارة ، والمحفزات
العبارة الثانية : تزيد المحفزات من سرعة التفاعلات بزيادة طاقة التنشيط .
العبارة الثالثة : يجب أن تصطدم جسيمات المواد المتفاعلة حتى يحدث تفاعل . أي العبارات السابقة صحيحة ؟
a .الأولى والثانية .
b .الثانية والثالثة .
c .الاولى والثالثة .
d .الاولى والثانية والثالثة .
الجواب : c .الاولى والثالثة .
السؤال : ما حجم الماء الذي يجب إضافته إلى 0.6ML من محلول قياسي تركيزه 0.050M لتخفيفه إلى محلول تركيزه 0.020M ؟
a- 15 ml
b-9.0 ml
c-6.0 ml
d-2.4ml
الجواب : b-9.0 ml
طريقة الحل : بداية نحسب عدد المولات في المحلول الأصلي

السؤال : أي الوحدات لا تستعمل للتعبير عن سرعة التفاعل ؟
𝑀/𝑚𝑖𝑛 .a
𝐿/𝑆 .b
𝑚𝑜𝑙/𝑚𝑙. ℎ .c
𝑚𝑜𝑙/𝑙. 𝑚𝑖𝑛 .d
الجواب : 𝐿/𝑆 .b
السؤال : أي أنواع القوى بين الجزيئية الآتية يعد الأقوى ؟
a.الرابطة الايونية
b .القوى ثنائية القطب .
c .قوى التشتت
d .الرابطة الهيدروجينية .
الجواب : a.الرابطة الايونية
استعمل الأشكال أدناه للإجابة عن السؤالين
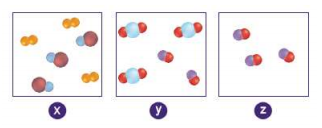
السؤال : أي العينات تحتوي على جزيئات غاز الأكسجين ؟
𝑋 .a
𝑦 .b
c .z
d. كل من Xو y
الجواب : 𝑋 .a
السؤال : أي العينات تحتوي على جزيئات فلوريد الماغنسيوم ؟
𝑋 .a
𝑦 .b
c .z
d. كل من Xو y
الجواب : 𝑦 .b
أسئلة الإجابات القصيرة
السؤال : افترض أن قانون السرعة العام هو : [B][A] = R. ما رتبة التفاعل بالنسبة لكل من المادة A والمادة B ؟ وما رتبة التفاعل الكلية
الجواب : رتبة التفاعل بالنسبة للمادةA هي الرتبة الأولى، رتبة التفاعل بالنسبة للمادة B هي الرتبة الثالثة، و رتبة التفاعل الكلية هي الرتبة الرابعة
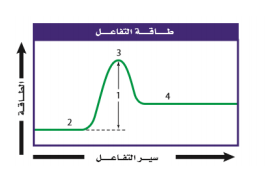
السؤال : يبين الشكل أعلاه منحنى طاقة تفاعل . إلام يشير كل رقم من الأرقام المبينة على الرسم ؟
الجواب :
1 : طاقة التنشيط
2 : طاقة المتفاعلات
3 : المعقد المنشط
3 : طاقة النواتج
السؤال : ( A ) = R تصف سرعة تفاعل من الرتبة الأولى . إذا تضاعف تركيز المادة A ماذا يطرأ على سرعة التفاعل ؟
الجواب : سوف تتضاعف سرعة التفاعل .
أسئلة الإجابات المفتوحة
تفاعل اليود والكلور في الحالة الغازية : I2 → cl2 + 2ICl
فإذا كان ( I2 )يساوي M 400.0 عند بداية التفاعل وأصبح M 300.0 بعد مضي min00.4
احسب متوسط سرعة التفاعل بوحدة mol/l.min .
الجواب :

.









