عرض بوربوينت الألدهيدات كيمياء 2-3 مسارات أ. ماجد الحكمي
مركبات الكربونيل الألدهيدات
سنتعلم اليوم كيف :
1- تذكر المركبات التي تحتوي على مجموعة الكربونيل.
2- تعرف الألدهيدات.
3- تعرف طريقة تسمية الألدهيدات.
4- تناقش خواص واستعمالات الألدهيدات.
التهيئة
هل النكهات الموجودة في قطعة حلوى نكهات طبيعية أم صناعية ؟
الألدهيدات
المركبات العضوية التي تحتوي على مجموعة الكربونيل
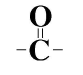
مجموعة الكربونيل :
هو الترتيب الذي ترتبط فيه ذرة أكسجين برابطة ثنائية مع ذرة الكربون .
أمثلة:
1- الألدهيدات.
2- الكيتونات.
الألدهيدات
هي مركبات عضوية تقع فيها مجموعة الكربونيل في آخر السلسلة وتكون مرتبطة مع ذرة كربون متصلة بذرة هيدروجين من الطرف الآخر .
الصيغة العامة
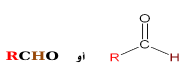
حيث أن R تمثل مجموعة الألكيل أو ذرة هيدروجين
التسمية بالطريقة الشائعة
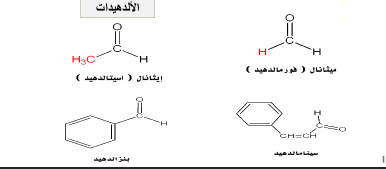
لبعض الألدهيدات أسماء عرفت بها نسبة إلى المصدر الذي اشتقت منه , مثل
| الاسم حسب المصدر | المركب |
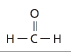 | ألدهيد النمل أو فورمالدهيد نسبة لحمض النمل ( Formica) التي تعني ( نمل ) باللغة اللاتينية. |
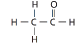 | ألدهيد الخل أو اسيتالدهيد نسبة لحمض الخل أسيتيك ( Acetum) التي تعني ( خل ) باللغة اللاتينية. |
التسمية بالطريقة النظامية IUPAC
1- نبدأ بترقيم الألدهيد من ذرة كربون المجموعة الكربونيل حيث تأخذ الرقم (1) ونستمر باتجاه أطول سلسلة من ذرات الكربون .
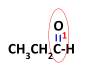
التسمية بالطريقة النظامية IUPAC
2- نسمي التفرعات إن وجدت كما تقدم في قواعد هذه الطريقة .
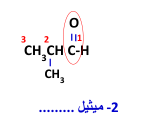
التسمية بالطريقة النظامية IUPAC
3- ننسب اسم الألدهيد إلى اسم الألكان في السلسة الأطول للمركب مضافًا إليها المقطع ( ال ) الدال على اسم مجموعة الكربونيل الألدهيدية .
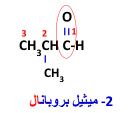
أمثلة
تدريب1
السؤال : سم المركبات التالية :
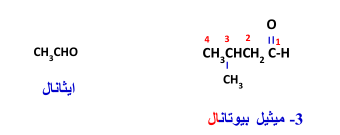
استعمالات الألدهيدات
1- تستعمل كميات كبيرة جداً من الفورمالدهيد للتفاعل مع اليوريا في صنع:
- نوع من الشمع المقاوم .
- المواد البلاستيكية
- الأزرار
- قطع غيار السيارات .
- غراء طبقات الخشب.
2- يستعمل محلول الفورمالدهيد في عمليات الحفظ لسنوات عديدة .
3- البنزالدهيد و الساليسالدهيد تعطي اللوز نكهته الطبيعية.
4-السينامالدهيد تعطي رائحة القرفة.
الخواص الفيزيائية للألدهيدات
1- الروابط الهيدروجينية
لا تكوَّن جزئياتها روابط هيدروجينية بعضها مع بعض لعدم وجود ذرات هيدروجين مرتبطة مباشرة مع ذرة الأكسجين .
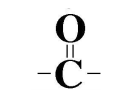
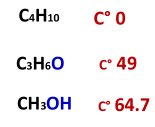
2- درجة الغليان
درجة غليانها اقل من الكحولات التي لها العدد نفسه من الكربونات لأنه لا يوجد بين جزيئاتها روابط هيدروجينية .
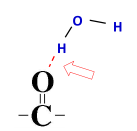
3- الذوبان
تذوب في الماء لأنه يمكن أن تكون روابط هيدروجينية مع الماء.
4- القطبية
تعتبر الألدهيدات قطبية لوجود رابطة قطبية بين الكربون و الأكسجين .
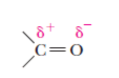
تدريب
السؤال : أيهما أعلى في درجة الغليان HCHO أم CH3OH ؟
الجواب :
درجة غليان CH3OH أعلى من HCHO
لأن جزيئات الألدهيدات لا تستطيع تكوين روابط هيدروجينية .
تقويم:
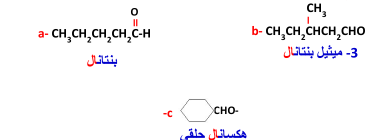
السؤال : سم المركبات التالية :
تعلمنا اليوم:
| تعريفه | تسميتها | خواصها | استخداماتها |
| هي مركبات عضوية تقع فيها مجموعة الكربونيل في آخر السلسلة وتكون مرتبطة مع ذرة كربون متصلة بذرة هيدروجين من الطرف الآخر . | 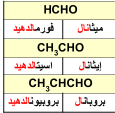 | القطبية الروابط الهيدروجينية الذوبان درجة الغليان |  |



